共有55例患者在我中心接受治疗。一名患者选择了最佳的支持性护理,另一名患者在接受治疗前死亡,两人都被排除在治疗反应分析之外。图1强调了患者中接受的治疗以及对治疗的反应。36例患者接受了高剂量甲氨蝶呤的化疗(改良De-Angelis方案)。其余患者因PS不良或其他原因接受替代化疗(替莫唑胺-地塞米松)。HDMTx循环的中位数为5(从1-5)。HDMTx治疗的总周期为140个。只有22/36(61.1%)的患者能够完成5个周期的HDMTx治疗。甲氨蝶呤毒性是患者无法接受较长的周期治疗的最常见原因。8例患者表现为神经毒性、肾功能衰竭或长期血细胞减少。这8例患者中有4例改为姑息治疗,以替莫唑胺为基础的化疗或rt的形式。3名患者在使用HDMTx后出现致命的危及生命的感染,均死于呼吸道感染。表1列述了HDMTx给药时出现的严重不良事件(定义为III级或以上不良事件)。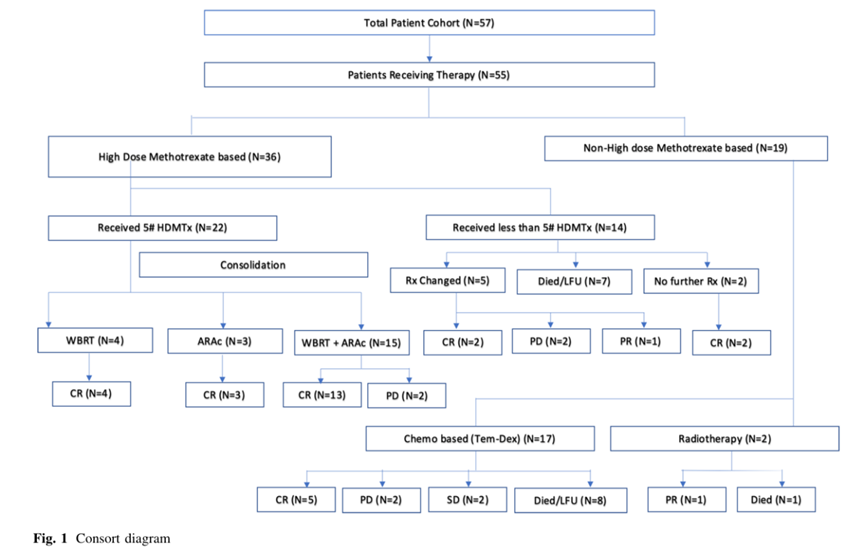
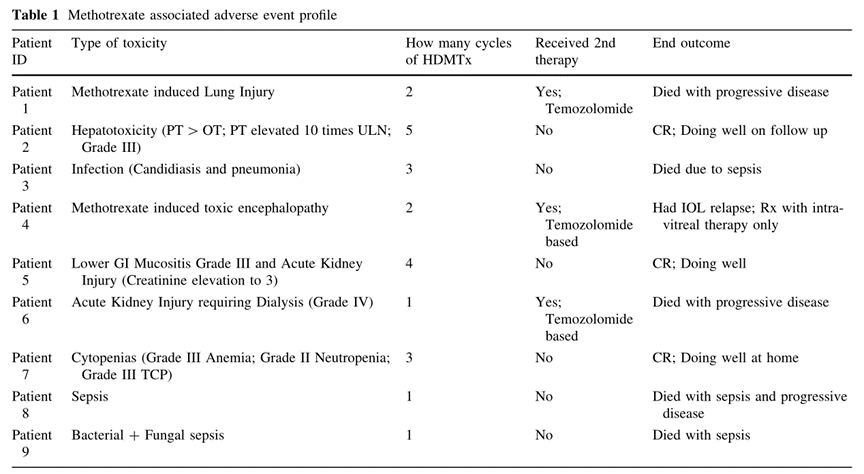
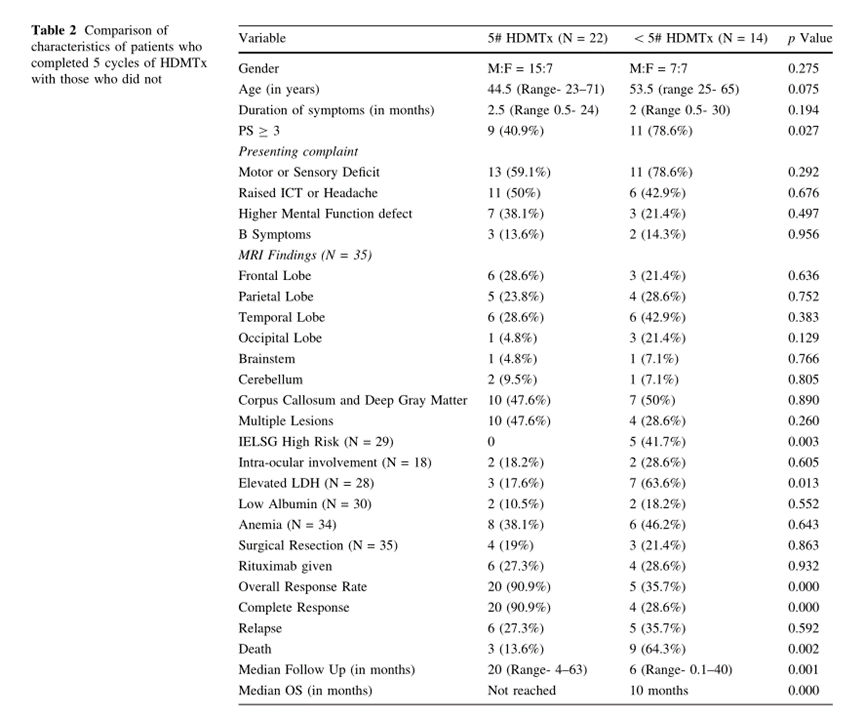
表2比较了完成和不能完成5个周期HDMTx治疗的患者。无法接受完整DeAngelis方案的患者综合表现较差(p = 0.027), IELSG评分较高(p = 0.003),基线时的LDH较高(p = 0.013)。这些患者年龄也显得较大,但并无统计学意义(p = 0.075)。19例患者由于高龄或由于经济限制接受替莫唑胺+地塞米松±利妥昔单抗方案。这些患者的中位年龄明显高于接受HDMTx治疗的患者(中位年龄67 vs 45岁;P = 0.000),大多数患者接受替莫唑胺为主的化疗(N = 17;89.5%),2例接受全脑放疗。14例患者(73.7%)在化疗的同时接受美罗华治疗。
我院2015年以后对PCNSL患者使用利妥昔单抗。2015年之后,接受治疗的46例患者中有24例(%)接受了利妥昔单抗作为治疗的一部分。其中10例患者接受R + DeAngelis方案,14例患者接受R +替莫唑胺+ Dexa方案。