
该研究是一项为期1年的回顾性单中心研究,评估了2020年1月至2020年12月在首尔国立大学盆唐医院接受TDM的患者的药代动力学和AKI发生率的关系。入组该研究的受试者均至少需要有两个可量化的万古霉素浓度。受试者必须在进行TDM咨询前7-28天里已经评估过eGFRs,且超过60 mL/min/1.73 m2,作为肾小球滤过率(eGFRs)变化的基线。该研究以治疗前后以肌酐值增加大于1.5倍或绝对值增加0.3 mg/dL为指标判定为AKI。数据分析中,AUC0-24和Cmin分别采用一点和两点抽样方法计算。在评测AKI的可预测性时,AUC0-24临界值设定为500、600和700 mg*h/L,Cmin设定为15和20 µg/mL。
研究共纳入407例符合纳入标准的TDM患者数据。其中,161例TDM病例被纳入分析。在分析的TDM数据中,可观察到万古霉素AUC0-24与肌酐变化率呈正相关。在评估AUC0-24 cutoff值与肌酐变化率之间的相关性时,在两种采样方法中,只有当cutoff值为500 mg*h/L时,与肌酐增加显著相关。
用ROC曲线估计AUC0-24的阈值时,一点法为524.26 mg*h/L,二点法为563.45 mg*h/L。这一临界值与之前建议的563至1300 mg*h/L相当或更低[3, 4]。用ROC曲线估计Cmin水平阈值时,一点法为8.95µg/mL,两点法为10.66µg/mL。这一临界值也低于先前建议的15至20µg/mL的治疗范围(图1)。
在多变量分析中,研究了其他可能影响AKI发生率的危险因素,并计算了万古霉素暴露阈值。除了AUC0-24 (563.45 mg*h/L)和低谷(8.95µg/mL)阈值外,其他危险因素与AKI之间均无关联。这表明计算出的阈值是AKI的独立预测因子,可以作为治疗目标范围的上限。
综上所述,该研究的结论基本与2020年修订的万古霉素TDM指南一致。计算得到的AUC0-24值为563.45 mg*h/L(两点抽样法),接近指南建议的上限600 mg*h/L。不过该研究也提示采用单点的Cmin也可以作为AKI的预测因子应用。这使得在患者不愿配合两点抽样AUC0-24检测时,可以采用Cmin来预防AKI的发生。
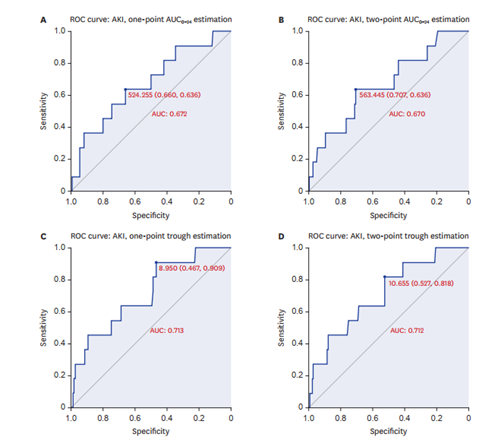
图表 1 预测AKI发生的AUC0-24和Cmin Cutoff值ROC曲线图。AUC为ROC曲线下面积